Perhatikan reaksi redoks berikut ini:
I2 + 2S2O3-2 → S4O6-2 +2I-
Dalam titrasi, sebanyak 40 mL larutan membutuhkan 4,0 x 10-3 mol I2 untuk bereaksi sempurna. Berapa konsentrasi larutan Na2S2O3 ?
A. 0,10
B. 0,16
C. 0,20
D. 0,32
E. 0,40
Pembahasan:
I2 + 2S2O3-2 → S4O6-2 +2I-
Berdasarkan persamaan reaksi yang setara di atas maka dalam titrasi tersebut jumlah mol S2O3-2 dapat dihitung berdasarkan perbandingan koefisien setara.
Mol S2O3-2 = 2/1 x 4,0 x 10-3 mol = 8,0 x 10-3 mol
Karena volume larutan S2O3-2 adalah 40 mL ~ 0,04 L, maka
[S2O3-2] = (8,0 x 10-3 mol) /(0,04 L) = 2 x 10-1 M ~ 0,2 M ← [Na2S2O3]
Jawaban C.
Soal Nomor 17:
Perhatikan reaksi redoks berikut ini:
C2H5OH +2Cr2O72- + 16H+ → CO2 + 4Cr3+ + 11H2O
Setiap atom karbon akan kehilangan:
A. 1 elektron
B. 2 elektron
C. 4 elektron
D. 6 elektron
E. 0 elektron
Pembahasan:
Bilangan oksidasi C dalam C2H5OH adalah -2 dan bilangan oksidasi C dalam CO2 adalah + 4, perubahan biloks C dari -2 ke +4 adalah 6, berarti ia akan melepaskan (kehilangan) 6 elektron.
Jawaban D.
Soal Nomor 18:
Sejumlah garam klorida lelehan dielektrolisis dengan suatu arus listrik 3,00 A. Jumlah deposit logam yang manakah akan memerlukan waktu elektrolisis terlama?
A. 50 g Mg
B. 75 g Al
C. 100 g Ca
D. 125 g Fe
E. Jawaban A, B, C dan D semuanya benar
Pembahasan:
Elektrolis suatu lelehan garam pada pada elektroda akan menghasilkan deposit logam (dari ion logamnya) yang biasanya akan menempel di elektroda dan gas klor (dari ion klorida) di sekitar elektroda lainnya.
Untuk menghitung lama waktu bisa menggunakan rumus sebagai berikut:
W = (e . i . t)/96500 → t = (W x 96500) : (e.i)
W = massa deposit logam (g); e = massa ekivalen (g); i = arus listrik (A); t = waktu (detik).
Mg2+ → Mg + 2e- →Ar Mg = 24 → massa ekivalen Mg = 24/2 = 12
Al3+ → Al + 3e- →Ar Al = 27 → massa ekivalen Al = 27/3 = 9
Ca2+ → Ca + 2e- →Ar Ca = 40 → massa ekivalen Ca = 40/2 = 20
Fe3+ → Fe + 3e- → Ar Fe = 56 → massa ekivalen Fe = 56/3 = 18,67
Fe2+ → Fe + 2e- → Ar Fe = 56 → massa ekivalen Fe = 56/2 = 28
t Mg = (50 g × 96500 C) : (12 g × 3,00 A) = 134.027,78 detik
t Al = (75 g × 96500 C) : (9 g × 3,00 A) = 268.055,56 detik
t Ca = (100 g × 96500 C) : (20 g × 3,00 A) = 168.833,33 detik
t Fe = (125 g × 96500 C) : (18,67 g × 3,00 A) = 215.363,33 detik
t Fe = (1250 g 96500 C) : (28 g 3,00 A) = 143.601,19 detik
Jadi yang memerlukan waktu paling lama adalah logam Al 75 g.
Jawaban B.
Soal Nomor 19:
Perhatikan Gambar sel elektrokimia beikut ini:
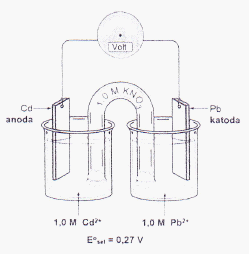
Bila sel tersebut dioperasikan, maka elektron akan mengalir kearah:
A. Elektroda Pb, dimana Pb akan dioksidasi
B. Elektroda Cd, dimana Cd akan dioksidasi
C. Elektroda Pb, dimana Pb2+ akan direduksi.
D. Elektroda Cd, dimana Cd2+ akan direduksi.
E. Elektroda Pb dimana Cd2+ akan dioksidasi
Pembahasan:
Mengalirnya elektron itu dari reaksi yang bisa menghasilkan elektron (reaksi oksidasi, terjadi di anoda) ke reaksi yang memerlukan elektron (reaksi reduksi, terjadi di katoda). Jadi elektron akan mengalir ke katoda Pb dan terjadi reaksi reduksi Pb2+ menjadi Pb.
Jawaban C.
Soal Nomor 20:
Nama IUPAC dari senyawa berikut adalah
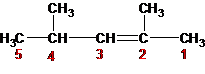
A. 2,3-dimetil-4-pentana
B. 1,1-dimetil-2-isopropiletena
C. 2,3-dimetil-2-pentana
D. 2,4-dimetil-2-pentena
E. 2,2-di metil-5-pentana
Pembahasan:
Tata nama berdasar IUPAC harus dimulai dari sisi di mana ikatan rangkap berada pada nomor urut C yang terkecil.
Jawaban D.








No comments:
Post a Comment