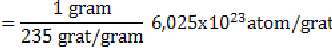Dahsyatnya Energi Nuklir
Posted by pada 20 September 2011
Istilah “nuklir” merupakan
kata yang sangat menakutkan bagi beberapa orang. Hal ini tidak
mengherankan karena istilah tersebut dikenalkan kepada dunia melalui
hancurnya dua kota di Jepang, Hiroshima dan Nagasaki. Hancurnya dua kota
tersebut mengakhiri pergolakan perang dunia II dimana Jepang menyerah
tanpa syarat kepada sekutu.
Bom yang dijatuhkan di Jepang, merupakan prinsip dari reaksi fisi yakni reaksi pembelahan isotop unsur-unsur berat menjadi menjadi dua inti yang bermasa sedang. Reaksi fisi dapat berlangsung secara spontan dan berlangsung secara induksi (menembak inti menggunakan suatu partikel) biasanya menggunakan neutron. Walaupun demikian tidak semua isotop unsur-unsur berat mengalami reaksi fisi. Reaksi fisi membebaskan energi yang besar baik dalam bentuk radiasi maupun energi kinetik hasil-hasil fisi.
Reaksi fisi yang terjadi pada bom nuklir tidak dapat dikendalikan, sehingga sekali meledak energi yang dihasilkan akan menghancurkan semua yang ada hingga mencapai keadaan yang stabil. Sedangkan reaksi fisi dalam reaktor nuklir dapat dikendalikan dengan cara menyerap kelebihan neutron sehingga reaksi fisi berantai dapat dihentikan.
Energi yang dihasilkan dari reaksi inti atau reaksi nuklir atau pembelahan inti membentuk unsur-unsur lain yang lebih stabil disebut energi nuklir. Energi yang dihasilkan pada suatu reaksi inti dihitung peratom, artinya satu atom saja sudah dapat menghasilkan energi.
Misalkan menghitung jumlah energi yang dihasilkan dari pembakaran 1 gram uranium-235.
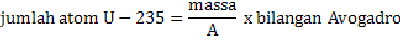
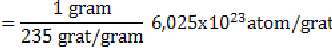
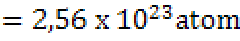
Bom yang dijatuhkan di Jepang, merupakan prinsip dari reaksi fisi yakni reaksi pembelahan isotop unsur-unsur berat menjadi menjadi dua inti yang bermasa sedang. Reaksi fisi dapat berlangsung secara spontan dan berlangsung secara induksi (menembak inti menggunakan suatu partikel) biasanya menggunakan neutron. Walaupun demikian tidak semua isotop unsur-unsur berat mengalami reaksi fisi. Reaksi fisi membebaskan energi yang besar baik dalam bentuk radiasi maupun energi kinetik hasil-hasil fisi.
Reaksi fisi yang terjadi pada bom nuklir tidak dapat dikendalikan, sehingga sekali meledak energi yang dihasilkan akan menghancurkan semua yang ada hingga mencapai keadaan yang stabil. Sedangkan reaksi fisi dalam reaktor nuklir dapat dikendalikan dengan cara menyerap kelebihan neutron sehingga reaksi fisi berantai dapat dihentikan.
Energi yang dihasilkan dari reaksi inti atau reaksi nuklir atau pembelahan inti membentuk unsur-unsur lain yang lebih stabil disebut energi nuklir. Energi yang dihasilkan pada suatu reaksi inti dihitung peratom, artinya satu atom saja sudah dapat menghasilkan energi.
Misalkan menghitung jumlah energi yang dihasilkan dari pembakaran 1 gram uranium-235.