Ikatan Logam, Sifat-Sifat Logam dan Alloy
Ikatan Logam dan sifat-sifat Logam
Logam atau
metal mememiliki beberapa karakter umum yaitu wujud padat, menunjukkan
kilap, massa jenis tinggi, titik didih dan titik lebur tinggi, konduktor
panas dan listrik yang baik, kuat atau keras namun mudah dibentuk
misalnya dapat ditempa (malleable) dan direnggangkan (ductile).
Walaupun demikian terdapat beberapa sifat yang menyimpang misalnya raksa
pada suhu kamar merupakan satu-satunya logam yang berwujud padat dan
hingga saat ini belum diketahui mengapa raksa berwujud cair.
Selain itu titik leleh beberapa unsur logam sangat rendah yaitu Hg, Cs
dan Rb dengan titik didih berturut-turut adalah -38,83 °C, 29°C dan 39°C
dan Li dan K memiliki massa jenis yang rendah yaitu 0,534 dan 0,86
g/mL.
Emas, perak dan platina disebut logam mulia, sedangkan emas, tembaga dan perak sering disebut sebagai logam mata uang, karena ketiga unsur ini dipadukan untuk membuat koin-koin mata uang. Dikatakan sebagai logam mulia karena ketiga logam ini sukar teroksidasi dengan sejumlah besar pereaksi.
Selain dikenal
logam mulia dikenal pula logam berat (heavy metal) adalah logam dengan
massa jenis lima atau lebih, dengan nomor atom 22 sampai dengan 92. Raksa, kadmium, kromium dan timbal merupakan beberapa contoh logam berat.
Logam-logam berat dalam jumlah yang banyak artinya melebihi kadar
maksimum yang ditetapkan, sangat berbahaya bagi kesehatan manusia karena
dapat menyebabkan kanker (bersifat karsinogen).
Ikatan Logam
Berdasarkan sifat umum logam dapat disimpulkan bahwa ikatan logam ternyata bukan merupakan ikatan ion maupun ikatan kovalen.
Ikatan logam didefinisikan berdasarkan model awan elektron atau lautan
elektron yang didefinisikan oleh Drude pada tahun 1900 dan disempunakan
oleh Lorents pada tahun 1923.
Berdasarkan
teori ini, logam di anggap terdiri dari ion-ion logam berupa bola-bola
keras yang tersusun secara teratur, berulang dan disekitar ion-ion logam
terdapat awan atau lautan elektron yang dibentuk dari elektron valensi
dari logam terkait.
Awan elektron
yang terbentuk berasal dari semua atom-atom logam yang ada. Hal ini
disebabkan oleh tumpang tindih (ovelap) orbital valensi dari atom-atom
logam (orbital valensi = orbital elektron valensi berada). Akibatnya elektron-elektron yang ada pada orbitalnya dapat berpindah ke orbital valensi atom tetangganya. Karena
hal inilah elektron-elektron valensi akan terdelokaslisasi pada semua
atom yang terdapat pada logam membentuk awan atau lautan elektron yang
bersifat mobil atau dapat bergerak.
Dari
teori awan atau lautan elektron ikatan logam didefinisikan sebagai gaya
tarik antara muatan positif dari ion-ion logam (kation logam) dengan
muatan negatif yang terbentuk dari elektron-elektron valensi dari
atom-atom logam. Jadi logam yang memiliki elektron valensi lebih banyak
akan menghasilkan kation dengan muatan positif yang lebih besar dan awan
elektron dengan jumlah elektron yang lebih banyak atau lebih rapat. Hal
ini menyebabkan logam memiliki ikatan yang lebih kuat dibanding logam
yang tersusun dari atom-atom logam dengan jumlah elektron valensi lebih
sedikit.
Misalnya logam magnesium yang memiliki 2 elektron valensi. Berdasarkan model awan elektron, logam aluminium dapat dianggap terdiri dari ion Al2+
yang tersusun secara teratur, berulang dan disekitarnya terdapat awan
atau lautan elektron yang dibentuk dari elektron valensi magnesium,
seperti pada Gambar.
Gambar Model awan elektron dari lagom magnesium
Logam dapat
dapat ditempa, direntangkan, tidak rapuh dan dapat dibengkokkan, karena
atom-atom logam tersusun secara teratur dan rapat sehingga ketika diberi
tekanan atom-atom tersebut dapat tergelincir di atas lapisan atom yang
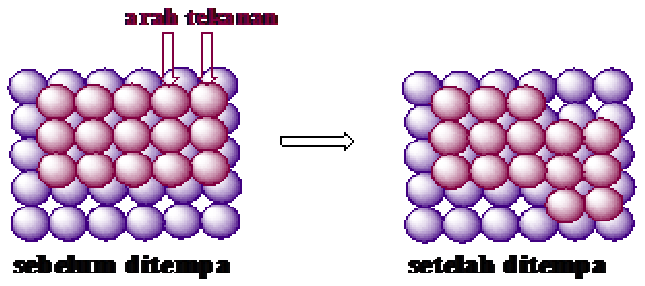
lain seperti yang ditunjukan pada Gambar.
Gambar perpindahan atom pada suatu logam ketika diberi tekanan atau ditempa
Dari gambar
menjelaskan mengapa logam dapat ditempa ataupun direntangkan, karena
pada logam semua atom sejenis sehingga atom-atom yang bergeser saat
diberi tekanan seolah-olah tetap pada kedudukan yang sama.
Keadaan ini
berbeda dengan ikatan ionik. Dalam kristal ionik, gaya pengikatnya
adalah gaya tarik antar ion yang bermuatan positif dengan ion yang
bermuatan negatif. Sehingga ketika kristal ionik diberi tekanan akan
terjadi pergeseran ion positif dan negatif yang dapat menyebabkan ion
positif berdekatan dengan ion positif dan ion negatif dengan ion negatif. Keadaan ini mengakibatkan terjadi gaya tolak antar ion-ion sejenis sehingga kristal ionik menjadi retak kemudian pecah.
Titik Didih dan Titik Lebur Logam
Titik didih dan titik lebur logam berkaitan langsung dengan kekuatan ikatan logamnya.
Titik didih dan titik lebur logam makin tinggi bila ikatan logam yang
dimiliki makin kuat. Dalam sistem periodik unsur, pada satu golongan
dari atas kebawah, ukuran kation logam dan jari-jari atom logam makin
besar.
Hal ini
menyebabkan jarak antara pusat kation-kation logam dengan awan
elektronnya semakin jauh, sehingga gaya tarik elektrostatik antara
kation-kation logam dengan awan elektronnya semakin lemah. Hal ini dapat dilihat pada titik didih dan titik lebur logam alkali.
|
Logam |
Jari-jari atom logam (pm) |
Kation logam |
Jari-jari kation logam (pm) |
Titik lebur (°C) |
Titik didih (°C) |
|
Li |
157 |
Li+ |
106 |
180 |
1330 |
|
Na |
191 |
Na+ |
132 |
97,8 |
892 |
|
K |
235 |
K+ |
165 |
63,7 |
774 |
|
Rb |
250 |
Rb+ |
175 |
38,9 |
688 |
|
Cs |
272 |
Cs+ |
188 |
29,7 |
690 |
Daya Hantar Listrik Logam
Sebelum logam
diberi beda potensial, elektron valensi yang membentuk awan elektron
bergerak ke segala arah dengan jumlah yang sama banyak.
Apabila pada logam diberi beda potensial, dengan salah satu ujung logam
ditempatkan elektroda positif (anoda) dan pada ujung yang lain
ditempatkan ujung negatif (katoda), maka jumlah elektron yang bergerak
ke anoda lebih banyak dibandingkan jumlah elektron yang bergerak ke
katoda sehingga terjadi hantaran listrik.
a
Daya Hantar Panas Logam
Berdasarkan
model awan elektron, apabila salah satu ujung dari logam dipanaskan maka
awan elektron ditempat tersebut mendapat tambahan energi termal.
Karena awan elektron bersifat mobil, maka energi termal tersebut dapat
ditransmisikan ke bagian-bagian lain dari logam yang memiliki temperatur
lebih rendah sehingga bagian tersebut menjadi panas.
Kilap Logam
Permukaan logam yang bersih dan halus akan memberikan kilap atau kilau (luster) tertentu. Kilau logam berbeda dengan kilau unsur nonlogam. Kilau logam dapat dipandang dari segala sudut sedangkan kilau nonlogam hanya dipandang dari sudut tertentu.
Logam akan
tampak berkilau apabila sinar tampak mengenai permukaannya. Hal ini
disebabkan sinar tampak akan menyebabkan terjadinya eksitasi
elektron-elektron bebas pada permukaan logam.
Eksitasi
elektron yaitu perpindahan elektron dari keadaan dasar (tingkat energi
terendah) menuju ke keadaan yang lebih tinggi (tingkat energi lebih
tinggi). Elektron yang tereksitasi dapat kembali ke keadaan dasar dengan memantulkan energi dalam bentuk radiasi elektromagnetik. Energi yang dipancarkan inilah yang menyebabkan logam tampak berkilau.
Aloi atau Alloy
Logam-logam
selalu dijumpai dalam kehidupan sehari-hari, misalnya rangka jendela,
peralatan-peralatan rumuh tangga, rangka pesawat maupun maupun bahan
lain yang menggunakan logam.
Bahan-bahan logam tersebut bukan hanya dibuat dari satu jenis unsur
logam tetapi telah dicampur atau ditambah dengan unsur-unsur lain yang
disebut aloi atau sering disebut lakur atau paduan.
Aloi terbentuk
apabila leburan dua atau lebih macam logam dicampur atau leburan suatu
logam dicampur dengan unsur-unsur nonlogam dan campuran tersebut tidak
saling bereaksi serta masih menunjukan sifat sebagai logam setelah
didinginkan.
Aloi dibagi menjadi dua macam yaitu aloi selitan dan aloi substitusi. Disebut aloi selitan bila jari-jari atom unsur yang dipadukan sama atau lebih kecil dari jari-jari atom logam. Sedangkan aloi substitusi terbentuk apabila jari-jari unsur yang dipadukan lebih besar dari jari-jari atom logam.
Baca Juga :





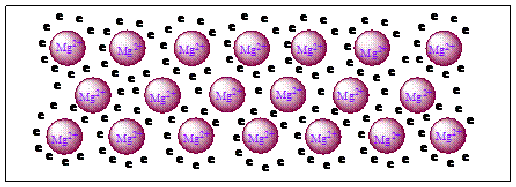



No comments:
Post a Comment